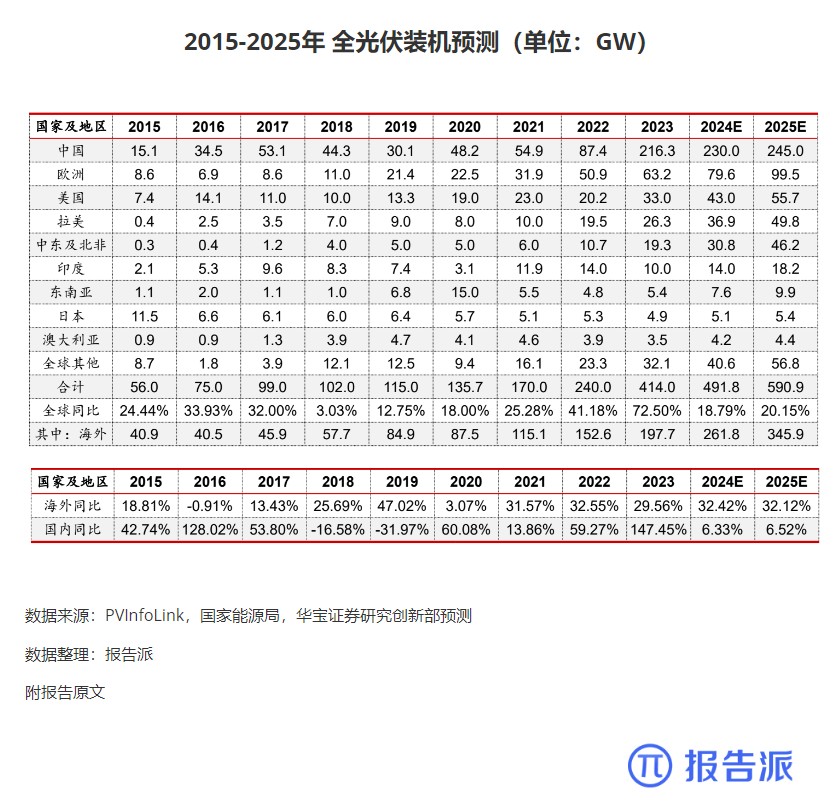
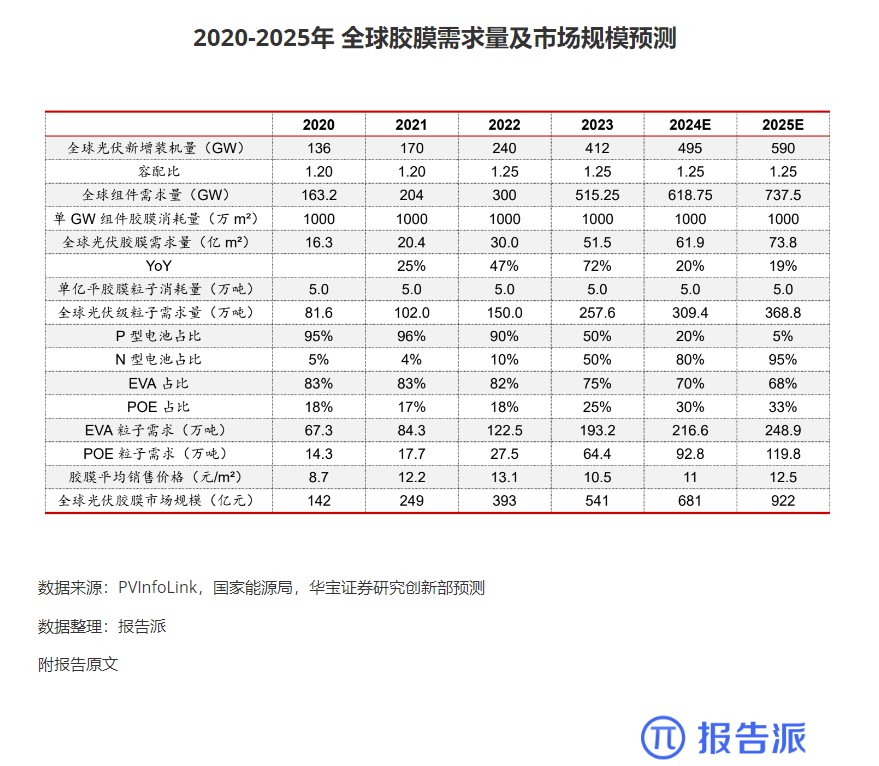
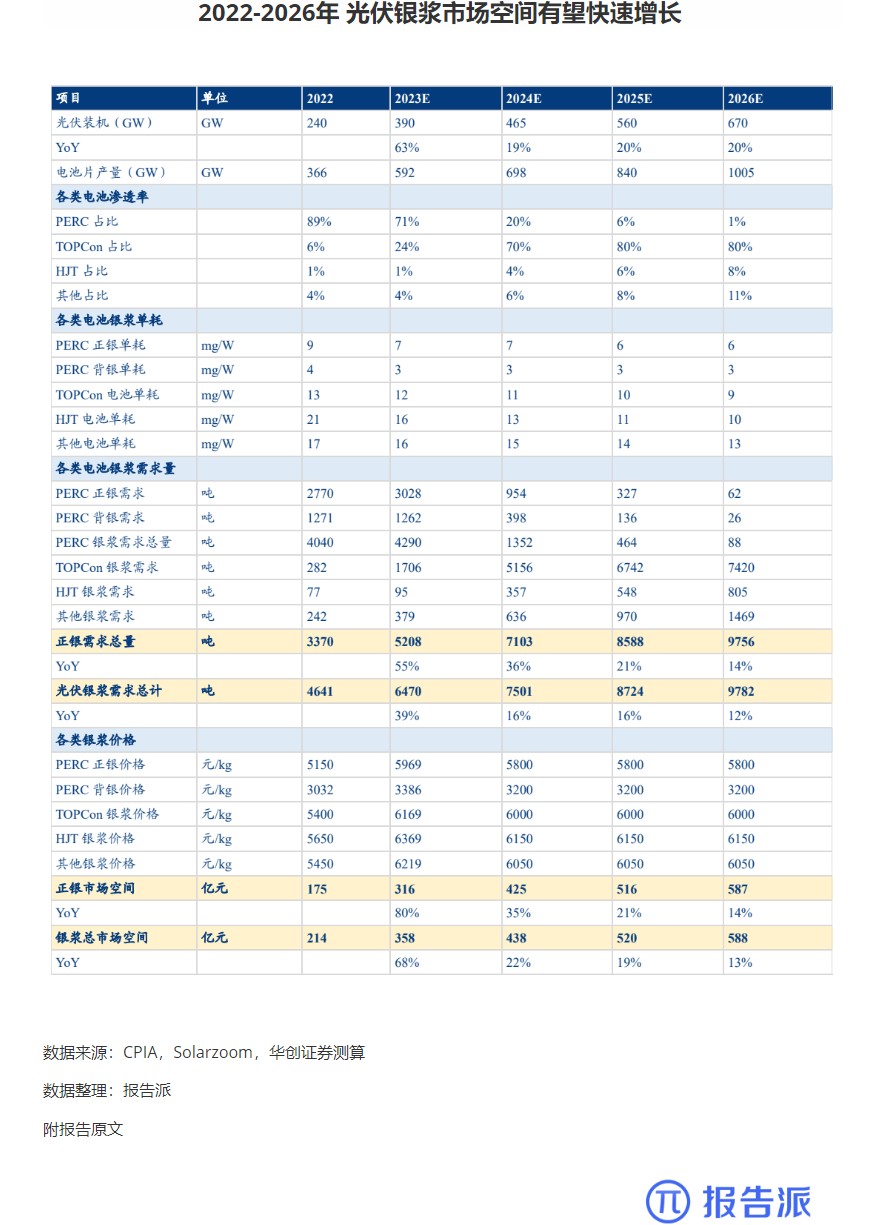
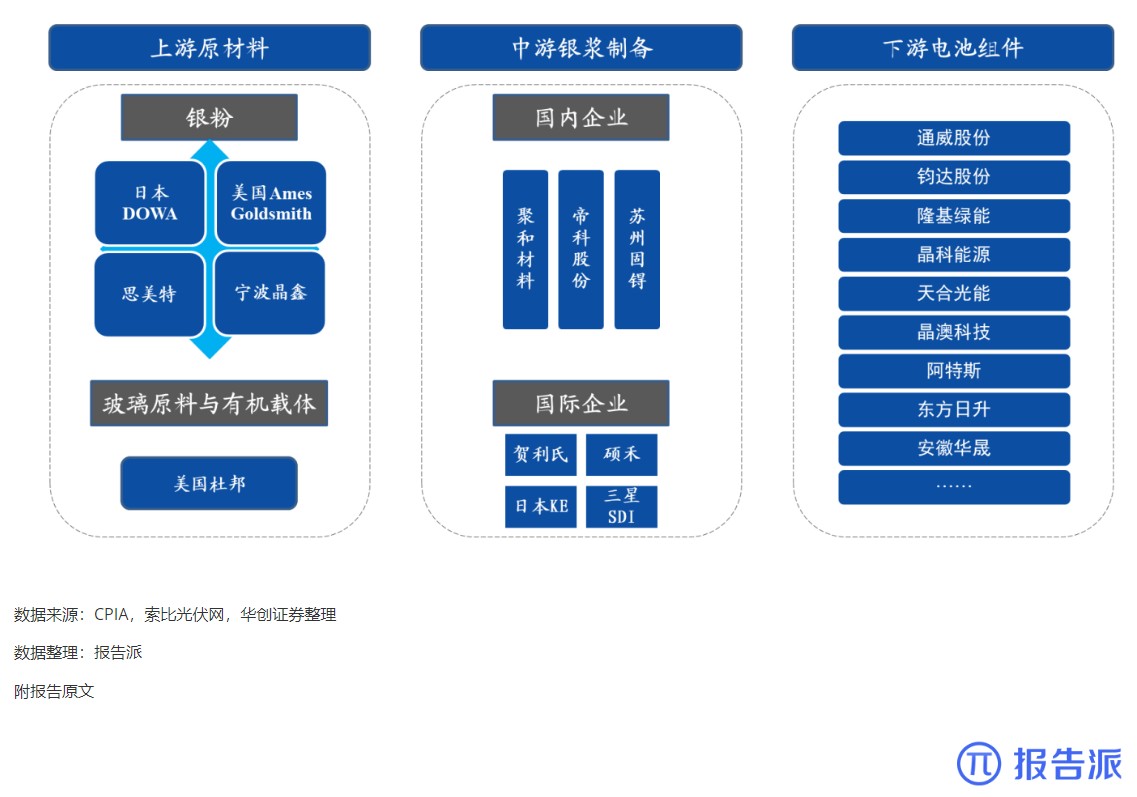
| 2024年05月全球监管机构批准药品——TarlatamabFDA加速批准tarlatamab(10mg)用于治疗铂类药物化疗期间或化疗后疾病进展的广泛期小细胞肺癌( ES-SCLC )成人患者,这是第一个也是唯一一个用于治疗ES-SCLC的T细胞接合器疗法,也是第一种且唯一一种获批的靶向DLL3的双特异性T细胞衔接抗体此项加速批准是基于2期DeLLphi-301临床试验(NCT05060016)结果,其中ORR达40%tarlatamab 是一种新型CD3×DLL3双特异性 T 细胞接合(BiTE),它通过与肿瘤细胞上的 DLL3 和 T 细胞上的CD3结合而起作用,从而触发T细胞依赖性抗肿瘤免疫。 DLL3 是一种在 ~85-96% 的SCLC细胞表面表达的蛋白质,但在健康细胞上的表达极少,因此DLL3是具有治疗SCLC 较大潜力的靶点。 图2临床结果有效性数据(部分)有效性数据:10 mg tarlatamab治疗组的主要终点ORR达40%,次要终点mPFS达4.9个月,mOS达14.3个月,mDOR为9.7 个月。
|